2021年度药品审评报告
2021年,国家药品监督管理局药品审评中心(以下简称药审中心)受理注册申请11658件,同比增长13.79%。受理需技术审评的注册申请9235件,同比增长29.11%,包括需经技术审评后报送国家局审批的注册申请2180件,需经技术审评后以国家局名义作出行政审批的注册申请7051件,需经技术审评后送国家药品监督管理局医疗器械技术审评中心、以医疗器械作用为主的药械组合产品的注册申请4件。受理无需技术审评直接以国家局名义作出行政审批的注册申请2423件。2017-2021年注册申请受理量可见下图。
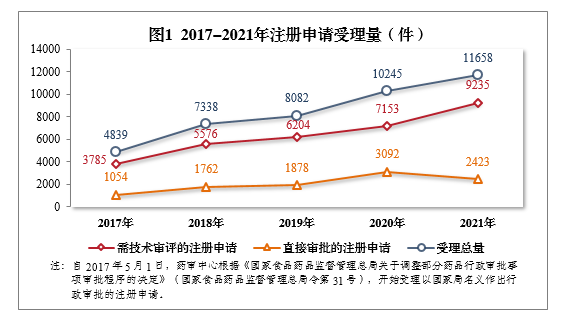
根据《国家药监局关于进一步完善药品关联审评审批和监管工作有关事宜的公告》(2019年第56号)要求,2021年受理原料药注册申请1313件,同比增长2.98%。
2021年批准IND 2108件,同比增长46.90%;建议批准NDA 323件,同比增长55.29%;建议批准ANDA 1003件,同比增长9.26%;批准一致性评价申请1080件,同比增长87.18%。建议批准境外生产原研药1876个品种。
临床急需境外新药81个品种中,截至2021年底,已有54个品种提出注册申请,51个品种获批上市,按审评时限审结率(以下简称按时限审结率)100%。
批准的药物按重点给出示例:
1、新冠病毒疫苗和新冠肺炎治疗药物:
(1)新型冠状病毒灭活疫苗(Vero细胞)(北京科兴中维生物技术有限公司)、新型冠状病毒灭活疫苗(Vero细胞)(国药集团中国生物武汉生物制品研究所有限责任公司),适用于预防新型冠状病毒感染所致的疾病(COVID-19)。
(2)重组新型冠状病毒疫苗(5型腺病毒载体),为首家获批的国产腺病毒载体新冠病毒疫苗,适用于预防由新型冠状病毒感染引起的疾病(COVID-19)。
(3)清肺排毒颗粒、化湿败毒颗粒、宣肺败毒颗粒,即“三方”品种,为《新型冠状病毒肺炎诊疗方案(试行第九版)》推荐药物,清肺排毒颗粒用于感受寒湿疫毒所致的疫病,化湿败毒颗粒用于湿毒侵肺所致的疫病,宣肺败毒颗粒用于湿毒郁肺所致的疫病。“三方”品种均来源于古代经典名方,是新冠肺炎疫情暴发以来,在武汉抗疫临床一线众多院士专家筛选出有效方药清肺排毒汤、化湿败毒方、宣肺败毒方的成果转化,也是《国家药监局关于发布〈中药注册分类及申报资料要求〉的通告》(2020年第68号)后首次按照“中药注册分类 3.2类 其他来源于古代经典名方的中药复方制剂”审评审批的品种。“三方”品种的获批上市为新冠肺炎治疗提供了更多选择,充分发挥了中医药在疫情防控中的作用。
(4)安巴韦单抗注射液(BRII-196)、罗米司韦单抗注射液(BRII-198),为我国首家获批拥有自主知识产权新冠病毒中和抗体联合治疗药物,上述两个药品可治疗新型冠状病毒肺炎(COVID-19),联合用于治疗轻型和普通型且伴有进展为重型(包括住院或死亡)高风险因素的成人和青少年(12—17岁,体重≥40kg)新型冠状病毒感染(COVID-19)患者,其中,青少年(12—17岁,体重≥40kg)适应症人群为附条件批准,其获批上市为新冠肺炎治疗提供了更多选择。
2、中药新药:
(1)益气通窍丸,具有益气固表,散风通窍的功效,适用于治疗对季节性过敏性鼻炎中医辨证属肺脾气虚证。本品为黄芪、防风等14种药味组成的原6类中药新药复方制剂,在中医临床经验方基础上进行研制,开展了随机、双盲、安慰剂平行对照、多中心临床试验,其获批上市为季节性过敏性鼻炎患者提供了一种新的治疗选择。
(2)益肾养心安神片,功能主治为益肾、养心、安神,适用于治疗失眠症中医辨证属心血亏虚、肾精不足证,症见失眠、多梦、心悸、神疲乏力、健忘、头晕、腰膝酸软等,舌淡红苔薄白,脉沉细或细弱。本品为炒酸枣仁、制何首乌等10种药味组成的原6类中药新药复方制剂,在中医临床经验方基础上进行研制,开展了随机、双盲、安慰剂平行对照、多中心临床试验,其获批上市为失眠症患者提供了一种新的治疗选择。
(3)银翘清热片,功能主治为辛凉解表,清热解毒,适用于治疗外感风热型普通感冒,症见发热、咽痛、恶风、鼻塞、流涕、头痛、全身酸痛、汗出、咳嗽、口干,舌红、脉数。本品为金银花、葛根等9种药味组成的1.1类中药创新药,在中医临床经验方基础上进行研制,开展了多中心、随机、双盲、安慰剂/阳性药平行对照临床试验,其获批上市为外感风热型普通感冒患者提供了一种新的治疗选择。
(4)玄七健骨片,具有活血舒筋,通脉止痛,补肾健骨的功效,适用于治疗轻中度膝骨关节炎中医辨证属筋脉瘀滞证的症状改善。本品为延胡索、全蝎等11种药味组成的1.1类中药创新药,基于中医临床经验方基础上进行研制,通过开展随机、双盲、安慰剂平行对照、多中心临床试验,获得安全性、有效性证据,其获批上市将为患者提供一种新的治疗选择。
(5)芪蛭益肾胶囊,具有益气养阴,化瘀通络的功效,适用于治疗早期糖尿病肾病气阴两虚证。本品为黄芪、地黄等10种药味组成的1.1类中药创新药,基于中医临床经验方基础上进行研制,通过开展随机、双盲、安慰剂平行对照、多中心临床试验,获得安全性、有效性证据,其获批上市将为患者提供新的治疗选择。
(6)坤心宁颗粒,具有温阳养阴,益肾平肝的功效,适用于治疗女性更年期综合征中医辨证属肾阴阳两虚证。本品为地黄、石决明等7种药味组成的1.1类中药创新药,基于中医临床经验方基础上进行研制,通过开展随机、双盲、安慰剂平行对照、多中心临床试验,获得安全性、有效性证据,其获批上市将为患者提供新的治疗选择。
(7)虎贞清风胶囊,具有清热利湿,化瘀利浊,滋补肝肾的功效,适用于治疗轻中度急性痛风性关节炎中医辨证属湿热蕴结证。本品为虎杖、车前草等4种药味组成的1.1类中药创新药,在中医临床经验方基础上进行研制,开展了随机、双盲、安慰剂平行对照、多中心临床试验,获得安全性、有效性证据,其获批上市将为患者提供新的治疗选择。
(8)解郁除烦胶囊,具有解郁化痰、清热除烦的功效,适用于治疗轻、中度抑郁症中医辨证属气郁痰阻、郁火内扰证。本品种为栀子、姜厚朴等8种药味组成的1.1类中药创新药,在中医临床经验方基础上进行研制,处方根据中医经典著作《金匮要略》记载的半夏厚朴汤和《伤寒论》记载的栀子厚朴汤化裁而来,开展了随机、双盲、阳性对照药(化学药品)、安慰剂平行对照、多中心临床试验,获得安全性、有效性证据,其获批上市将为患者提供新的治疗选择。
(9)七蕊胃舒胶囊,具有活血化瘀,燥湿止痛的功效,适用于治疗轻中度慢性非萎缩性胃炎伴糜烂湿热瘀阻证所致的胃脘疼痛。本品为三七、枯矾等4种药味组成的1.1类中药创新药,在医疗机构制剂基础上进行研制,开展了随机、双盲、阳性药平行对照、多中心临床试验,其获批上市为慢性胃炎患者提供了新的治疗选择。
(10)淫羊藿素软胶囊,适用于治疗不适合或患者拒绝接受标准治疗、且既往未接受过全身系统性治疗的、不可切除的肝细胞癌,患者外周血复合标志物满足以下检测指标的至少两项:AFP≥400 ng/mL;TNF-α<2.5pg/mL;IFN-γ≥7.0pg/mL。本品为从中药材淫羊藿中提取制成的1.2类中药创新药,其获批上市为肝细胞癌患者提供了新的治疗选择。
3、罕见病药物:
(1)布罗索尤单抗注射液,适用于治疗成人和1岁以上儿童患者的X连锁低磷血症(XLH)。X连锁低磷血症属罕见病,目前尚无有效治疗药物。本品种属临床急需境外新药名单品种,为以成纤维细胞生长因子23(FGF23)抗原为靶点的一种重组全人源IgG1单克隆抗体,可结合并抑制FGF23活性从而使血清磷水平增加,其获批上市为患者提供了新的治疗选择。
(2)醋酸艾替班特注射液,适用于治疗成人、青少年和≥2岁儿童的遗传性血管性水肿急性发作。遗传性血管性水肿属罕见病,近半数患者会出现上呼吸道黏膜水肿,引发窒息进而危及生命,已被纳入国家卫生健康委员会等五部门联合公布的《第一批罕见病目录》。本品种属临床急需境外新药名单品种,为缓激肽B2受体的竞争性拮抗剂,其获批上市可为我国遗传性血管性水肿患者的预防发作提供安全有效的药物。
(3)注射用艾诺凝血素α,适用于成人和儿童B型血友病(先天性IX因子缺乏)患者的以下治疗:按需治疗以及控制出血事件;围手术期的出血管理;常规预防,以降低出血事件的发生频率。血友病B属遗传性、出血性罕见病,目前国内尚无长效重组人凝血因子Ⅸ进口或上市。本品种属临床急需境外新药名单品种,为首个在国内申报进口的长效重组人凝血因子IX产品,其获批上市为患者提供了新的治疗选择。
(4) 注射用司妥昔单抗,适用于治疗人体免疫缺陷病毒(HIV)阴性和人疱疹病毒8型(HHV-8)阴性的多中心卡斯特曼病(MCD)成人患者。MCD是一种以淋巴组织生长为特征的罕见病,多数患者出现多器官损害且预后差,部分患者会转化为恶性淋巴瘤,已被纳入国家卫生健康委员会等五部门联合公布的《第一批罕见病目录》。本品种属临床急需境外新药名单品种,其获批上市为患者提供了治疗选择。
(5)奥法妥木单抗注射液,适用于治疗成人复发型多发性硬化(RMS),包括临床孤立综合征、复发缓解型多发性硬化和活动性继发进展型多发性硬化。多发性硬化(MS)是免疫介导的慢性中枢神经系统疾病,已被纳入国家卫生健康委员会等五部门联合公布的《第一批罕见病目录》。本品为抗人CD20的全人源免疫球蛋白G1单克隆抗体,其获批上市为患者提供了治疗选择。
4、儿童用药:
(1)利司扑兰口服溶液用散,适用于治疗2月龄及以上患者的脊髓性肌萎缩症(SMA)。SAM是由于运动神经元存活基因1(SMN1)突变导致SMN蛋白功能缺陷所致的遗传性神经肌肉病,是造成婴幼儿死亡的常染色体隐性遗传疾病之一,已被纳入国家卫生健康委员会等五部门联合公布的《第一批罕见病目录》。本品种为治疗儿童罕见病的1类创新药,可直接靶向疾病的潜在分子缺陷,增加中枢组织和外周组织的功能性SMN蛋白的产生,其获批上市可为SMA患者提供新的治疗选择。
(2)达妥昔单抗β注射液,适用于治疗≥12月龄的高危神经母细胞瘤和伴或不伴有残留病灶的复发性或难治性神经母细胞瘤的儿童患者。神经母细胞瘤为儿童常见的恶性肿瘤之一,尚无免疫治疗产品获批上市。本品种属临床急需境外新药名单品种,其获批上市可丰富儿童患者的治疗选择。
(3)顺铂注射液,此前已批准适用于小细胞与非小细胞肺癌、非精原细胞性生殖细胞癌、晚期难治性卵巢癌、晚期难治性膀胱癌、难治性头颈鳞状细胞癌、胃癌、食管癌的姑息治疗,此次新增批准了儿童用法用量,其获批上市保障了儿童临床合理用药。
(4)盐酸氨溴索喷雾剂,适用于治疗2-6岁儿童的痰液粘稠及排痰困难。本品种为适合儿童使用剂型的改良型新药,相对于口服制剂,可以避免遗撒和呕吐,对于年龄小且不配合服药的儿童而言,具有更好的顺应性,其获批上市可丰富儿童患者的治疗选择。
(5)盐酸头孢卡品酯颗粒,适用于儿童对头孢卡品敏感的菌所致的下列感染:皮肤软组织感染、淋巴管和淋巴节炎、慢性脓皮病;咽炎、喉炎、扁桃体炎(包括扁桃体周炎,扁桃体周脓肿)、急性支气管炎、肺炎;膀胱炎、肾盂肾炎;中耳炎、鼻窦炎;猩红热。本品种为第三代口服头孢菌素类抗菌药物,剂型具有较高的用药依从性,适合儿童尤其是婴幼儿使用,其获批上市可为儿童患者提供一种有效的治疗选择。
5、公共卫生用药:
(1)四价流感病毒裂解疫苗,适用于3岁及以上人群预防疫苗相关型别的流感病毒引起的流行性感冒。本品种为使用世界卫生组织推荐的甲型(H1N1和H3N2)和乙型(B/Victoria和B/Yamagata)流行性感冒病毒株制成的裂解疫苗,国内既往使用的流感疫苗以三价流感病毒裂解疫苗为主,本品种在此基础上增加了一种乙型流感抗原,以增加对乙型流感的抗体保护率和阳转率,其获批上市有助于进一步缓解四价流感疫苗供不应求的矛盾。
(2)ACYW135群脑膜炎球菌多糖结合疫苗(CRM197载体),适用于预防A群、C群、Y群和W135群脑膜炎奈瑟球菌引起的流行性脑脊髓膜炎。本品种为国内首个批准上市的四价脑膜炎多糖结合疫苗,其获批上市可填补国内2岁以下儿童无Y群、W135群脑膜炎多糖结合疫苗可用的空白。
(3)冻干人用狂犬病疫苗(Vero细胞),适用于预防狂犬病。目前国内仅两家企业疫苗获批四剂免疫程序,其余均为五剂免疫程序,本品种同时申报五剂免疫程序和2-1-1四剂免疫程序,其获批上市可进一步缓解狂犬病疫苗市场短缺现象。
6、抗肿瘤药物:
(1)甲磺酸伏美替尼片,适用于既往经EGFR酪氨酸激酶抑制剂治疗时或治疗后出现疾病进展,并且经检测确认存在EGFR T790M突变阳性的局部晚期或转移性非小细胞性肺癌(NSCLC)成人患者的治疗。本品种是我国自主研发并拥有自主知识产权的1类创新药,为第三代表皮生长因子受体(EGFR)激酶抑制剂,其获批上市为患者提供了新的治疗选择。
(2)普拉替尼胶囊,适用于既往接受过含铂化疗的转染重排(RET)基因融合阳性的局部晚期或转移性非小细胞性肺癌(NSCLC)成人患者的治疗。本品为受体酪氨酸激酶RET(Rearranged during Transfection)抑制剂的1类创新药,可选择性抑制RET激酶活性,可剂量依赖性抑制RET及其下游分子磷酸化,有效抑制表达RET(野生型和多种突变型)的细胞增殖,其获批上市为患者提供了新的治疗选择。
(3)赛沃替尼片,适用于治疗含铂化疗后疾病进展或不耐受标准含铂化疗的、具有间质-上皮转化因子(MET)外显子14跳变的局部晚期或转移性非小细胞肺癌成人患者。本品种是我国拥有自主知识产权的1类创新药,为我国首个获批的特异性靶向MET激酶的小分子抑制剂,可选择性抑制MET激酶的磷酸化,对MET 14号外显子跳变的肿瘤细胞增殖有明显的抑制作用,其获批上市为患者提供了新的治疗选择。
(4)舒格利单抗注射液,适用于联合培美曲塞和卡铂用于表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性的转移性非鳞状非小细胞肺癌患者的一线治疗,以及联合紫杉醇和卡铂用于转移性鳞状非小细胞肺癌患者的一线治疗。本品为重组抗PD-L1全人源单克隆抗体,可阻断PD-L1与T细胞上PD-1和免疫细胞上CD80间的相互作用,通过消除PD-L1对细胞毒性T细胞的免疫抑制作用,发挥抗肿瘤作用,其获批上市为患者提供了新的治疗选择。
(5)优替德隆注射液,适用于联合卡培他滨,治疗既往接受过至少一种化疗方案的复发或转移性乳腺癌患者。本品种是我国自主研发并拥有自主知识产权的1类创新药,为埃坡霉素类衍生物,可促进微管蛋白聚合并稳定微管结构,诱导细胞凋亡,其获批上市为患者提供了新的治疗选择。
(6)羟乙磺酸达尔西利片,适用于联合氟维司群,治疗既往接受内分泌治疗后出现疾病进展的激素受体阳性、人表皮生长因子受体2阴性的复发或转移性乳腺癌患者。本品种是一种周期蛋白依赖性激酶4和6(CDK4和CDK6)抑制剂的1类创新药,可降低CDK4和CDK6信号通路下游的视网膜母细胞瘤蛋白磷酸化水平,并诱导细胞G1期阻滞,从而抑制肿瘤细胞的增殖。其获批上市为患者提供了新的治疗选择。
(7)帕米帕利胶囊,适用于既往经过二线及以上化疗的伴有胚系BRCA(gBRCA)突变的复发性晚期卵巢癌、输卵管癌或原发性腹膜癌患者的治疗。本品种为PARP-1和PARP-2的强效、选择性抑制剂1类创新药,通过抑制肿瘤细胞DNA单链损伤的修复和同源重组修复缺陷,对肿瘤细胞起到合成致死的作用,尤其对携带BRCA基因突变的DNA修复缺陷型肿瘤细胞敏感度高。其获批上市为患者提供了新的治疗选择。
(8)甲苯磺酸多纳非尼片,适用于既往未接受过全身系统性治疗的不可切除肝细胞癌患者。本品种是我国自主研发并拥有自主知识产权的1类创新药,为多激酶抑制剂类小分子抗肿瘤药物,其获批上市为患者提供了一种新的治疗选择。
(9)注射用维迪西妥单抗,适用于至少接受过2种系统化疗的人表皮生长因子受体-2过表达局部晚期或转移性胃癌(包括胃食管结合部腺癌)患者的治疗。本品种为我国自主研发的创新抗体偶联药物(ADC),包含人表皮生长因子受体-2(HER2)抗体部分、连接子和细胞毒药物单甲基澳瑞他汀E(MMAE),其获批上市为患者提供了新的治疗选择。
(10)阿基仑赛注射液,适用于治疗既往接受二线或以上系统性治疗后复发或难治性大B细胞淋巴瘤成人患者(包括弥漫性大B细胞淋巴瘤非特指型、原发纵膈大B细胞淋巴瘤、高级别B细胞淋巴瘤和滤泡淋巴瘤转化的弥漫性大B细胞淋巴瘤)。本品种为我国首个批准上市的细胞治疗类产品,是一种自体免疫细胞注射剂,由携带CD19 CAR基因的逆转录病毒载体进行基因修饰的自体靶向人CD19嵌合抗原受体T细胞(CAR-T)制备,其获批上市为患者提供了新的治疗选择。
(11)瑞基奥仑赛注射液,适用于治疗经过二线或以上系统性治疗后成人患者的复发或难治性大B细胞淋巴瘤。本品种是我国首款自主研发的以及中国第二款获批上市的细胞治疗类产品,为靶向CD19的自体CAR-T细胞免疫治疗产品,其获批上市为患者提供了新的治疗选择。
(12)奥雷巴替尼片,适用于治疗任何酪氨酸激酶抑制剂耐药,并采用经充分验证的检测方法诊断为伴有T315I突变的慢性髓细胞白血病慢性期或加速期的成年患者。本品种为我国自主研发并拥有自主知识产权的1类创新药,是小分子蛋白酪氨酸激酶抑制剂,可有效抑制Bcr-Abl酪氨酸激酶野生型及多种突变型的活性,可抑制Bcr-Abl酪氨酸激酶及下游蛋白STAT5和Crkl的磷酸化,阻断下游通路活化,诱导Bcr-Abl阳性、Bcr-Abl T315I突变型细胞株的细胞周期阻滞和调亡,是国内首个获批伴有T315I突变的慢性髓细胞白血病适应症的药品,其获批上市为因T315I突变导致耐药的患者提供了有效的治疗手段。
(13)恩沃利单抗注射液,适用于不可切除或转移性微卫星高度不稳定(MSI-H)或错配修复基因缺陷型(dMMR)的成人晚期实体瘤患者的治疗,包括既往经过氟尿嘧啶类、奥沙利铂和伊立替康治疗后出现疾病进展的晚期结直肠癌患者以及既往治疗后出现疾病进展且无满意替代治疗方案的其他晚期实体瘤患者。本品种为我国自主研发的创新PD-L1抗体药物,为重组人源化PD-L1单域抗体Fc融合蛋白注射液,可结合人PD-L1蛋白,并阻断其与受体PD-1的相互作用,解除肿瘤通过PD-1/PD-L1途径对T细胞的抑制作用,调动免疫系统的抗肿瘤活性杀伤肿瘤,其获批上市为患者提供了新的治疗选择。
7、抗感染药物:
(1)阿兹夫定片,与核苷逆转录酶抑制剂及非核苷逆转录酶抑制剂联用,适用于治疗高病毒载量的成年HIV-1感染患者。本品种是新型核苷类逆转录酶和辅助蛋白Vif抑制剂的1类创新药,也是首个上述双靶点抗HIV-1药物,能够选择性进入HIV-1靶细胞外周血单核细胞中的CD4细胞或CD14细胞,发挥抑制病毒复制功能。其获批上市为HIV-1感染者提供了新的治疗选择。
(2)艾诺韦林片,适用于与核苷类抗逆转录病毒药物联合使用,治疗成人HIV-1感染初治患者。本品种为HIV-1新型非核苷类逆转录酶抑制剂的1类创新药,通过非竞争性结合HIV-1逆转录酶抑制HIV-1的复制,其获批上市为HIV-1感染患者提供了新的治疗选择。
(3)艾米替诺福韦片,适用于治疗慢性乙型肝炎成人患者。本品种是我国自主研发并拥有自主知识产权的1类创新药,为核苷类逆转录酶抑制剂,其获批上市为慢性乙型肝炎患者提供了新的治疗选择。
(4)甲苯磺酸奥马环素片、注射用甲苯磺酸奥马环素,适用于治疗社区获得性细菌性肺炎(CABP)、急性细菌性皮肤和皮肤结构感染(ABSSSI)。甲苯磺酸奥马环素为新型四环素类抗菌药,具有广谱抗菌活性,以及口服和静脉输注两种剂型,其获批上市丰富了患者的治疗选择,提高了药品可及性。
(5)康替唑胺片,适用于治疗对康替唑胺敏感的金黄色葡萄球菌(甲氧西林敏感和耐药的菌株)、化脓性链球菌或无乳链球菌引起的复杂性皮肤和软组织感染。本品种是我国自主研发并拥有自主知识产权的1类创新药,为全合成的新型噁唑烷酮类抗菌药,其获批上市为患者提供了新的治疗选择。
(6)苹果酸奈诺沙星氯化钠注射液,适用于治疗对奈诺沙星敏感的肺炎链球菌、金黄色葡萄球菌、流感嗜血杆菌、副流感嗜血杆菌、卡他莫拉菌、肺炎克雷伯菌、铜绿假单胞菌以及肺炎支原体、肺炎衣原体和嗜肺军团菌所致的成人(≥18岁)社区获得性肺炎。本品种为无氟喹诺酮类抗菌药,与含氟喹诺酮类抗菌药具有不同的作用位点,其获批上市可为患者提供新的治疗选择。
(7)注射用磷酸左奥硝唑酯二钠,适用于治疗肠道和肝脏严重的阿米巴病、奥硝唑敏感厌氧菌引起的手术后感染和预防外科手术导致的敏感厌氧菌感染。本品种属于最新一代硝基咪唑类抗感染药,其获批上市可为厌氧菌感染的治疗和预防提供新的治疗选择。
8、内分泌系统药物:
(1)西格列他钠片,适用于配合饮食控制和运动,改善成人2型糖尿病患者的血糖控制。本品种是我国自主研发并拥有自主知识产权的1类创新药,为过氧化物酶体增殖物激活受体(PPAR)全激动剂,能同时激活PPAR三个亚型受体(α、γ和δ),并诱导下游与胰岛素敏感性、脂肪酸氧化、能量转化和脂质转运等功能相关的靶基因表达,抑制与胰岛素抵抗相关的PPARγ受体磷酸化,其获批上市为患者提供了新的治疗选择。
(2)脯氨酸恒格列净片,适用于改善成人2型糖尿病患者的血糖控制。本品种是我国自主研发并拥有自主知识产权的1类创新药,为钠-葡萄糖协同转运蛋白2(SGLT2)抑制剂,通过抑制SGLT2,减少肾小管滤过的葡萄糖的重吸收,降低葡萄糖的肾阈值,从而增加尿糖排泄。其获批上市为患者提供新的治疗选择。
9、循环系统药物:
(1)海博麦布片,适用于作为饮食控制以外的辅助治疗,可单独或与HMG-CoA还原酶抑制剂(他汀类)联合用于治疗原发性(杂合子家族性或非家族性)高胆固醇血症,可降低总胆固醇、低密度脂蛋白胆固醇、载脂蛋白B水平。本品种为我国自主研发并拥有自主知识产权的1类创新药,可抑制甾醇载体Niemann-Pick C1-like1(NPC1L1)依赖的胆固醇吸收,从而减少小肠中胆固醇向肝脏转运,降低血胆固醇水平,降低肝脏胆固醇贮量,其获批上市为原发性高胆固醇血症患者提供了新的治疗选择。
10、血液系统药物:
(1)海曲泊帕乙醇胺片,适用于因血小板减少和临床条件导致出血风险增加的既往对糖皮质激素、免疫球蛋白等治疗反应不佳的慢性原发免疫性血小板减少症成人患者,以及对免疫抑制治疗疗效不佳的重型再生障碍性贫血(SAA)成人患者。本品种是我国自主研发并拥有自主知识产权的1类创新药,为小分子人血小板生成素受体激动剂,其获批上市为患者提供了新的治疗选择。
11、风湿性疾病及免疫药物:
(1)注射用泰它西普,适用于与常规治疗联合用于在常规治疗基础上仍具有高疾病活动的活动性、自身抗体阳性的系统性红斑狼疮(SLE)成年患者。本品种为我国自主研发的创新治疗用生物制品,可将B淋巴细胞刺激因子(BLyS)受体跨膜蛋白活化物(TACI)的胞外特定的可溶性部分,与人免疫球蛋白G1(IgG1)的可结晶片段(Fc)构建成的融合蛋白,由于TACI受体对BLyS和增殖诱导配体(APRIL)具有很高的亲和力,本品种可以阻止BLyS和APRIL与它们的细胞膜受体、B细胞成熟抗原、B细胞活化分子受体之间的相互作用,从而达到抑制BLyS和APRIL的生物学活性的作用,其获批上市为患者提供了新的治疗选择。
12、皮肤五官药物:
(1)阿普米司特片,适用于治疗符合接受光疗或系统治疗指征的中度至重度斑块状银屑病的成人患者。本品种属临床急需境外新药名单品种,是磷酸二酯酶4(PDE4)小分子抑制剂,可以通过抑制PDE4促使细胞内环磷酸腺苷(cAMP)含量升高,从而增加抗炎细胞因子,并下调炎症反应,其获批上市可为患者提供一种给药便利的新型替代治疗选择。
(文章来源,国家药品监督管理局 https://www.nmpa.gov.cn/directory/web/nmpa/xxgk/fgwj/gzwj/gzwjyp/20220601110541120.html)



